ღვინოში ერთ-ერთი ყველაზე მნიშვნელოვანი ფაქტორი წყალბადის იონების კონცენტრაციაა. ღვინის ფიზიკურ-ქიმიური მახასიათებლები, სენსორული ფაქტორები და მიკრო-ბიოლოგიური სტაბილურობაც კი, სწორედ ამ წყალბადის იონების რაოდენობაზეა დამოკიდებული. ამ იონების კონცენტრაცია ლოგარითმული კონცენტრაციით იზომება და შემოკლებით pH-ს ვეძახით.
pH=-log[H+]
pH მნიშვნელობები 0-დან 14-მდე დიაპაზონშია დაყოფილია, სადაც 7 ნეიტრალური სითხეა. 0-7 მაჩვენებელი მჟავა სითხეებია, 7-14 კი ტუტე სითხეები. კიდევ ერთხელ უნდა აღინიშნოს, რომ ეს მონაცემები ლოგარითმული სკალითაა შედგენილი, რაც ნიშნავს, რომ მაგალითად pH-ის მნიშვნელობა 3-ს და 4-ს შორის, ლოგარითმული დამოკიდებულების შედეგად, pH-3 10-ჯერ უფრო ძლიერი მჟავიანობის მაჩვენებელია, ვიდრე pH4. pH7 აქვს სუფთა წყალს. ღვინის pH ძირითადად 3-ს და 4-ს შორისაა.
ღვინოში ძირითადად გვხვდება სუსტი ორგანული მჟავები, კერძოდ ღვინის მჟავა, რძემჟავა, ლიმონმჟავა, ვაშლმჟავა და ძმარმჟავა. სუსტი მჟავები, ძლიერ მჟავებთან შედარებით, სუსტი დისოცირების ხარისხით გამოირჩევა, შესაბამისად წყალბადის იონების კონცენტრაციაც, ამ შემთხვევაში, შედარებით დაბალია. დისოცირების ხარისხი pK - დისოცირების მუდმივათი აღინიშნება, რომელიც სხვადასხვა მჟავას განსხვავებული მნიშვნელობის აქვს. სუსტ მჟავებში (ღვინოში შემავალი მჟავების შემთხვევაში) ეს კოეფიციენტი ძირითადად ძალიან მცირეა (0.0001, ან უფრო ნაკლები), შესაბამისად ღვინოში ამ მჟავების დისოცირება მიახლოებით 1%-ს შეადგენს.
წყალბადის იონის კონცენტრაცია vs. ტიტრული და ჯამური მჟავიანობა.
ხშირად ბევრი ადამიანი შედის შეცდომაში და pH-ს ჯამურ მჟავიანობასთან აიგივებს. სინამდვილეში, ამ ორს შორის ძალიან მნიშვნელოვანი სხვაობაა. როგორც ზემოთ აღვნიშნეთ, pH წყალბადის იონების (პროტონების) კონცენტრაციაა. ჯამური მჟავიანობა, როგორც თვითონ დასახელება გვეუბნება, სითხეში შემავალი მჟავების კონცენტრაციაა. მათი გაზომვის ტექნიკაც სხვადასხვანაირია. pH საკმაოდ მარტივი ხელსაწყოთი იზომება, რომელსაც pH მზომი ეწოდება. ამ ხელსაწყოს ღირებულება დაახლოებით 20 აშშ დოლარია (უფრო მაღალი სიზუსტის მოწყობილობები უფრო ძვირი ღირს) და მეღვინისთვის ძალიან მნიშვნელოვან საზომ ხელსაწყოს წარმოადგენს. ჯამური მჟავიანობის დადგენა კი ე.წ. ტიტრირების მეთოდით ხდება.
ჯამური მჟავიანობა ხარისხიანი ღვინის მისაღებად ძალიან მნიშვნელოვანი პარამეტრია. ღვინის მჟავიანობა ძირითადად 0.4-0.85%-ის ფარგლებში მერყეობს (4-7.5 გ/ლ ღვინის მჟავაზე გადაანგარიშებით), თუმცა მაღალხარისხიან ღვინოებში მჟავიანობა უმჯობესია 5.5-7.5 გ/ლ ფარგლებში იყოს. ამ მნიშვნელობაზე ნაკლები მჟავიანობის ღვინოს დაძველების დიდი პოტენციალი არ აქვს, ნაკლებადაა დაცული მიკრობიოლოგიური პრობლემებისგან და ასევე ორგანოლეპტიკური თვალსაზრისითაც შედარებით "დუნეა". ზედმეტად მაღალი მჟავიანობის მქონე ღვინო მიკრობიოლოგიურად უფრო სტაბილურია, თუმცა დასალევად უკვე არასასიამოვნო ხდება, განსაკუთრებით თუ მისი ბალანსი დარღვეულია.
და მაინც რისთვის გვჭირდება ღვინოსთან დაკავშირებული ამდენი ინფორმაცია და ანალიზები?
პირველ რიგში, ამ ანალიზების გაკეთების საჭიროება ჯერ კიდევ ყურძნის წვენში დგება, რათა ყურძნის სიმწიფის ხარისხი, ასევე მისგან მიღებული საბოლოო პროდუქტის - ღვინის პოტენციური ხარისხი განვსაზღვროთ, თუ როგორი დაბალანსებული იქნება ის. ამასთან ერთად, pH-ის გაზომვით დუღილის პროცესში მყოფი წვენისა და შემდეგ უკვე ღვინის მიკრობიოლოგიური სტაბილურობის ხარისხს ვიგებთ. სწორედ pH-ზეა დამოკიდებული თუ რა რაოდენობის გოგირდის დიოქსიდის დამატება იქნება საჭირო. რომ ღვინო მიკრობიოლოგიურად სტაბილური გახდეს. ხშირად მეღვინეები ამ პარამეტრებს უგულებელყოფენ და ზეპირად, მეგობრების თუ ახლობლების რჩევით, ღვინოში "გოგირდის" (კალიუმის მეტაბისულფიტის) იწყებენ, ღვინის სტაბილიზაციისთვის. ეს არასწორი პრაქტიკაა, რადგან, როგორც აღვნიშნეთ, ღვინის მიკრობიოლოგიური სტაბილიზაციისთვის საჭირო დასამატებელი გოგირდის დიოქსიდის რაოდენობა ღვინის pH-ზეა დამოკიდებული. ეს მახასიათებელი კი ყველა ღვინოში განსხვავებულია, შესაბამისად ზოგ ღვინოს შესაძლებელია საერთოდ არ სჭირდებოდეს გოგირდის დამატება, ზოგს კი უფრო მეტის დამატება სჭირდებოდეს და ამ რაოდენობამ თავისი ფუნქცია ვერ შეასრულოს.
აქედან გამომდინარე, pH-ის მნიშვნელობის გაზომვის შემდეგ, მეღვინეს ღვინის სტაბილურობის ხარისხის განსაზღვრა შეეძლება. აუცილებელი გოგირდის დიოქსიდის რაოდენობა კი ცხრილებში თუ ონლაინ კალკულატორებში უნდა მოიძიონ, რაც ინტერნეტში მარტივად ხელმისაწვდომია.
pH სპეციალური, მცირე ზომის მოწყობილობით იზომება, რომელსაც pH მეტრი ეწოდება. ეს მოწყობილობები სხვადასხვა ფასის და ხარისხისაა, ამაზონზე 15 დოლარის ფარგლებშიც კი ხელმისაწვდომია. ასეთი, შედარებით იაფფასიანი მოწყობილობები, დიდი სიზუსტით არ გამოირევა. თუმცა, არ ქონას ეს იაფფასიანი მოწყობილობა სჯობს. ამ მოწყობილობის შეძენისას, მთავარი გასათვალისწინებელი ფაქტორია, რომ მას 0.01 სიზუსტე ჰქონდეს, ანუ მთელი რიცხვის შემდეგ 2 დანაყოფს ზომავდეს. ამ ტიპის მოწყობილობების უმეტესობას დასაკალიბრირებელი ღილაკიც აქვს. ასევე, ინსტრუქციაც მოჰყვება - მათი დაკალიბრება როგორ უნდა მოხდეს. დაკალიბრება აუცილებელია, რათა პერიოდულად მეტ-ნაკლებად ზუსტი მნიშვნელობა მივიღოთ. გაზომვა ძალიან მარტივია. სატესტო სითხეს (ყურძნის წვენს ან ღვინოს) ჭურჭელში მოვათავსებთ, ამ სითხეში მზომ ხელსაწყოს ისე ჩავყოფთ, რომ სითხემ მინის ელექტროდი დაფაროს. მასში მოთავსების შემდეგ, ციფრულ დისპეიზე pH შედეგი ცვლილებას (გაზრდას ან შემცირებას) დაიწყებს. საბოლოო მნიშვნელობა დასტაბილურების შემდეგ იქნება (ამას ზოგჯერ 2-3 წუთი შეიძლება დასჭირდეს, თუმცა, უმეტეს შემთხვევაში, საშუალოდ 1 წუთი გრძელდება).
რაც შეეხება საერთო მჟავიანობის გაზომვას, აქ ცოტა უფრო მეტი სამუშაოა ჩასატარებელი. ამისთვის, პირველ რიგში, შემდეგი რეაქტივები და მოწყობილობები დაგვჭირდება:
პროცედურა:
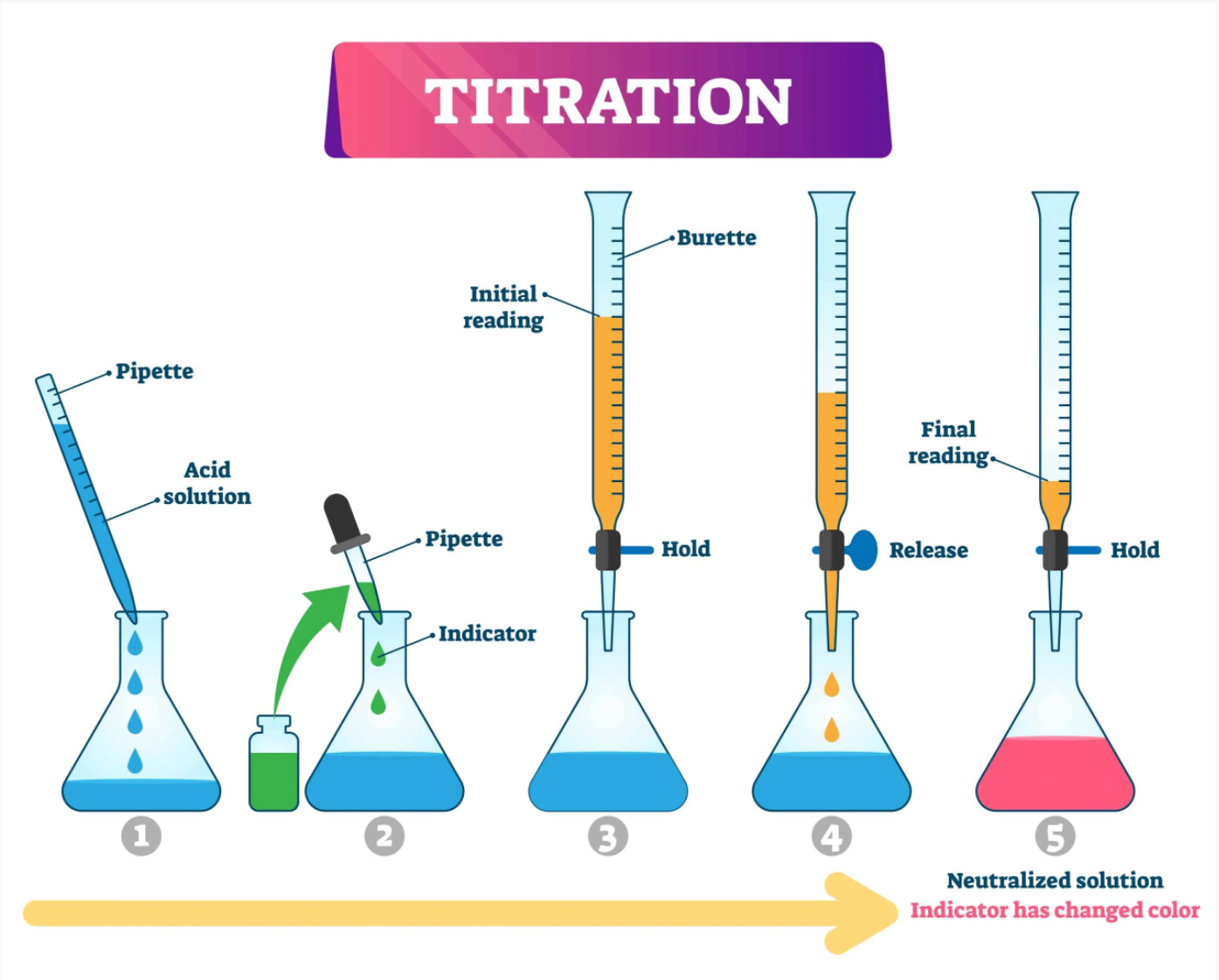
მინის გამჭვირვალე სინჯარაში, ან სხვა ფორმის ჭურჭელში სატესტო სითხეს (ყურძნის წვენს ან ღვინოს) ვათავსებთ. ვამატებთ 2-3 წვეთ ფენოფთალეინის ხსნარს, კარგად ავურევთ და ნატრიუმის ტუტის ხსნარით ვიწყებთ გატიტვრას, სანამ სატესტო ხსნარი ფერს არ შეიცვლის. გატიტვრა ძალიან ნელა ხდება, თითო წვეთის დამატებით, პარალელურად, მუდმივი მორევით. გარკვეული რაოდენობის სატიტრი ხსნარის დამატების შემდეგ, სატესტო სითხის ფერი ცვლილებას იწყებს. როდესაც სითხე ფერს შეიცვლის, მეტ გასატიტრ ხსნარს აღარ ვამატებთ. 10-15 წამი ველოდებით, თუ ფერი შენარჩუნდა და საწყის ფერს არ დაუბრუნდა, მაშინ გატიტვრა დასრულებულია. თუ ფერი საწყის ფერს დაუბრუნდა, მაშინ გატიტვრას ისევ წვეთ-წვეთის დამატებით ვაგრძელებთ. როდესაც ვნახავთ რომ ფერი დასტაბილურდა, ჩავინიშნავთ თუ რა რაოდენობის გასატიტრი სითხე დაიხარჯა და ეს მონაცემები შემდეგ ფორმულაში, საერთო მჟავიანობის დასადგენად, შეგვყავს:
საერთო მჟავიანობა (TA გ/ლ)=(დახარჯული გასატიტრი (NaOH) ხსნარის რაოდენობა მლ-ში)*7.5/(ღვინის ნიმუშის მოცულობა მლ-ში).
მაგალითად, თუ გასატესტად ავიღებთ 10მლ ღვინოს, ხოლო გასატიტრად დაიხარჯა 8 მლ NaOH და ამ მონაცემებს შევიყვანთ ფორმულაში, მაშინ მივიღებთ:
TA (გ/ლ)=8*7.5/10=6 გ/ლ.
© ღვინის კლუბი/vinoge.com